Cuando hablamos de hidruros hacemos mención de aquellos compuestos químicos que se forman con hidrógeno y otro elemento que puede ser cualquiera que se encuentre dentro de la tabla periódica de los elementos, es decir un metal o un no metal.
El principal elemento de estos compuestos es el hidrógeno que se encuentra en estado libre en todo el planeta. Sin embargo, es difícil de encontrar en los gases emitidos por las erupciones volcánica o en los gases naturales. Existen algunos elementos de la tabla periódica que tienen la capacidad de absorber al hidrógeno tal como sucede con el Platino (Pt), el Tantalio (Ta), el Cobalto (Co), el Hierro (Fe) y el Níquel (Ni).
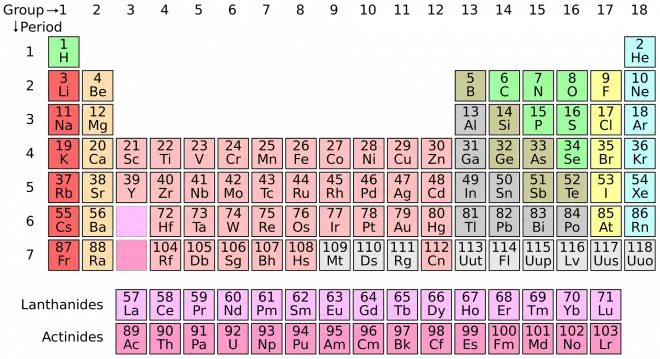
Los hidruros se forman cuando se une uno o más átomos de hidrógeno con cualquier elemento de la tabla periódica.
En la atmósfera es posible encontrar al menos una parte de Hidrógeno (H) por cada millón de partes del aire. Sin embargo, los expertos en la materia afirman que existen capas superficiales en las que el Hidrógeno es mucho más abundante.
Características de los hidruros
Los hidruros se pueden dividir en dos grupos, los metálicos en los cuales el hidrógeno se combina con cualquier metal de la tabla periódica y los no metálicos que están compuestos por un no metal además de, por supuesto, el hidrógeno.
Los hidruros se escriben colocando primero el elemento y después el hidrógeno. A continuación se intercambian los números de oxidación. Por ejemplo en el caso del trihidrudo de aluminio o AlH3, el numero de oxidación del hidrógeno, – que es -1- se coloca como el subíndice correspondiente al aluminio. Por otro lado, el aluminio cuenta con un número de oxidación de +3, pero este número se coloca al lado del hidrógeno como subíndice.
El intercambio de números de oxidación en el caso de los hidruros no metálicos se realiza con el menor número de oxidación.
Nomenclatura de los hidruros
La nomenclatura de los hidruros se escribe de la siguiente manera:
- Un ácido + no metal+ le prefijo hídrico: por ejemplo ácido sulfhídrico.
- No metal+ el prefijo URO + de hidrógeno: por ejemplo, sulfuro de hidrógeno.
Si son elementos que tienen una sola valencia se nombran con el sufijo ICO.
En el caso de dos valencias, a la menor se le incluye el sufijo OSO y en la mayor ICO.
Si el elemento tiene tres valencias, el menor se nombra como hidruro HIPO…OSO, la valencia del medio se escribe con el sufijo OSO y la mayor con el sufijo IPO.
Si el elemento tiene 4 valencias, la menos se nombra como hidruro HIPO…OSO; la segunda con el sufijo OSO; la tercera con el sufijo ICO y la cuarta valencia con el sufijo PER…ICO.
Ejemplos de hidruros metálicos
LiH (Hidruro de Litio)
Hidruro de Sodio (NaH)
Hidruro de Potasio (KH)
Hidruro de Berilio (BeH2)
Hidruro de Calcio (CaH2)
Hidruro de Magnesio (MgH2)
Hidruro de Hierro (FeH3)
Ejemplos de hidruros no metálicos o hidrácidos
Agua (H2O)
Amoniaco (NH3)
Borano (BH3)
Fosfamina (PH3)
Cloruro de Hidrógeno (HCl)
Sulfuro de Hidrógeno (H2S)
Metano (CH4)
